
De izquierda a derecha: Xavier Trepat, Pau Guillamat y Marino Arroyo.
Un estudio liderado por el Instituto de Bioingeniería de Cataluña (IBEC), la Universitat Politècnica de Catalunya – BarcelonaTech (UPC) y el Centro Internacional de Métodos Numéricos en Ingeniería (CIMNE), en colaboración con el European Molecular Biology Laboratory (EMBL) de Barcelona, permite obtener tejidos vivos capaces de deformarse de forma controlada para generar estructuras tridimensionales reproducibles.
La investigación, publicada en la revista Science, presenta una nueva estrategia para “programar” los cambios de forma de los tejidos, controlando, mediante patrones químicos, cómo se orientan las células. Los expertos plantean los objetivos del estudio como una vía para diseñar superficies vivas que cambian de forma por sí mismas, con potenciales aplicaciones que van desde la ingeniería de tejidos hasta la robótica biohíbrida.
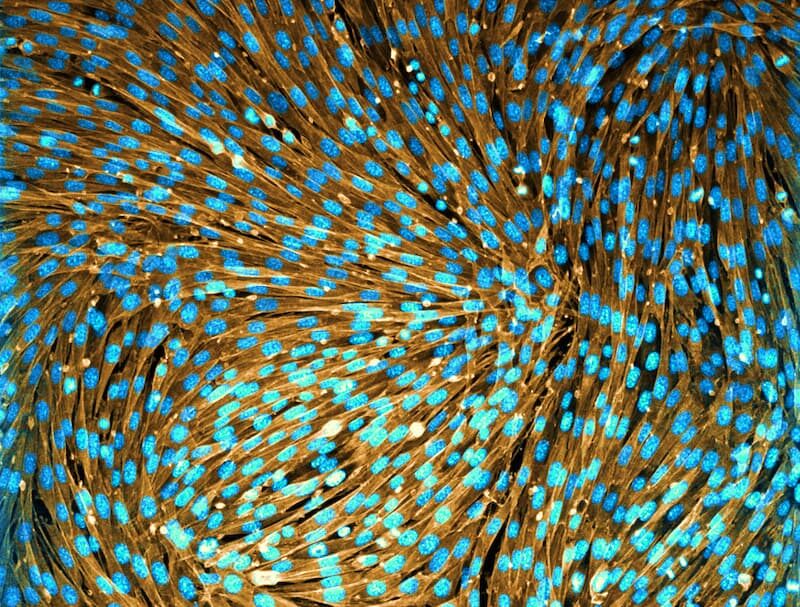
Imagen confocal de una monocapa celular nemática
Células que se alinean y dan forma a tejidos
Los tejidos biológicos formados por células alargadas tienden a autoorganizarse generando dominios multicelulares donde todas las células se orientan en la misma dirección, como las fibras de un hilo en un tejido textil. Este es el denominado orden nemático.
En ocasiones, este orden se rompe en puntos concretos, llamados defectos topológicos, que actúan como puntos de concentración de fuerzas, capaces de influir en cómo crecen, migran o incluso se deforman los tejidos. “La orientación de las células controla las fuerzas, y las fuerzas pueden controlar la generación de una forma en tres dimensiones”, explica Pau Guillamat, investigador del grupo de Dinámica Integrativa de Células y Tejidos del IBEC, y primer autor del estudio.
Para guiar estas fuerzas, el equipo utilizó el micropatronaje químico: “dibujaron” sobre superficies planas unas líneas de una proteína a la que las células se adhieren, rodeadas de zonas con un polímero al que las células no se adhieren. Gracias a estos patrones, las células se alinean siguiendo las líneas, creando el “mapa” de orientaciones deseado. Esto permitió imponer defectos topológicos en posiciones exactas, algo que la naturaleza genera de forma espontánea, pero de manera desordenada.
Vídeo de un tejido transformándose en una forma 3D que recuerda a una rosa.
Simulaciones que predicen la forma final
Marino Arroyo, catedrático de la UPC, investigador del CIMNE y colíder del estudio, lidera el grupo Interfaces de materiales blandos y vivos del CIMNE, que desarrolla modelos computacionales de células, tejidos y materiales bioinspirados para estudiar la invasión del cáncer, la mecánica epitelial y la morfogénesis, uniendo la mecanobiología con aplicaciones biomédicas.
Para profundizar en el origen de las fuerzas y formas de los tejidos, así como para poder predecirlas, el equipo de Arroyo desarrolló modelos teóricos y simulaciones que permiten anticipar cómo un patrón concreto de orientaciones celulares acabaría transformándose en una forma tridimensional específica.
Según explica, “nuestros modelos nos han permitido examinar diferentes hipótesis y finalmente identificar el mecanismo por el que la orientación de las células conduce al plegado tridimensional de los tejidos. Además, proporcionan una relación cuantitativa entre patrón nemático y forma”, lo que confirma que el sistema puede utilizarse como una plataforma predictiva de diseño morfológico de tejidos.
Monocapa celular deformada, mostrada como una visualización renderizada
Un abanico de aplicaciones
Esta investigación es una prueba de concepto, pero abre la puerta a muchas aplicaciones, como la ingeniería de tejidos, para crear estructuras tridimensionales sin necesidad de andamios artificiales; la robótica biohíbrida, que podría utilizar tejidos vivos deformables como actuadores biológicos; o el diseño de materiales vivos inteligentes, superficies vivas capaces de reconfigurar su forma y, potencialmente, sus propiedades funcionales.
Además de sus posibles aplicaciones, esta metodología permite estudiar fenómenos presentes en la biología real, como la formación de órganos o el comportamiento de algunos tumores. “Es una herramienta perfecta para entender cómo los patrones de orientación celular influyen en la mecánica y evolución de tejidos complejos”, afirma Xavier Trepat, profesor de investigación ICREA en el IBEC y colíder de la investigación.
Artículo de referencia
Pau Guillamat, Waleed Mirza, Pradeep K. Bal, Manuel Gómez-González, Pere Roca-Cusachs, Marino Arroyo, Xavier Trepat. Guidance of cellular nematic elastomers into shape-programmable living surfaces. Science (2026). DOI: 10.1126/science.adz9174








